长久以来,放疗因可以杀灭淋巴细胞被认为有免疫抑制作用。然而,近些年来,越来越多的研究证明,放疗可以使肿瘤新抗原释放增多,而且可以促进肿瘤微环境中的淋巴细胞浸润增加以及促炎细胞因子分泌增多,从而使「冷肿瘤」转化为「热肿瘤」,诱导肿瘤免疫原性细胞死亡,增强抗肿瘤免疫应 答1 。
「远隔效应(abscopal effect)」最早是在 1953 年由 Doctor Mole 提出的,是指除了受照射的肿瘤灶以外,非受照射的病灶也缩小的现象。单纯使用放疗产生远隔效应病例比较少见,可能和单纯放疗不足以产生足够的保护性免疫反应有关。然而随着免疫治疗在临床应用的增加,放疗联合免疫治疗出现远隔效应的个案报道逐渐增 多2 。
本文笔者通过分享 Marco F3 等在《Immunotherapy》发表的一例晚期喉癌病例跨线使用纳武利尤单抗联合纵隔淋巴结转移灶放疗,取得了极好的「远隔效应」,并获得了长期生存的个案报道,和各位同道一起学习「远隔效应」的机制、适宜人群以及今后可能的研究方向。
病例展示
患者为一名 58 岁男性,2015 年接受了全喉切除术联合双侧颈部淋巴结清扫及辅助放疗。2020 年 7 月,患者因局部淋巴结复发和骨转移,接受了一线紫杉醇联合卡铂及西妥昔单抗全身治疗。
2020 年 12 月,患者全身 CT 显示主动脉后上方、左侧气管旁有一病理性淋巴结,与食管紧密相邻,淋巴结最大径约 25 mm;主动脉旁有一巨大的转移淋巴结,大小约 65*25 mm,同时骨盆和骶髂关节见多处溶骨性病变(图 1)。考虑患者病情进展,患者随后接受了针对疼痛部位的骨盆转移灶放疗以及二线的纳武利尤单抗 240 mg 每 2 周一次免疫治疗。
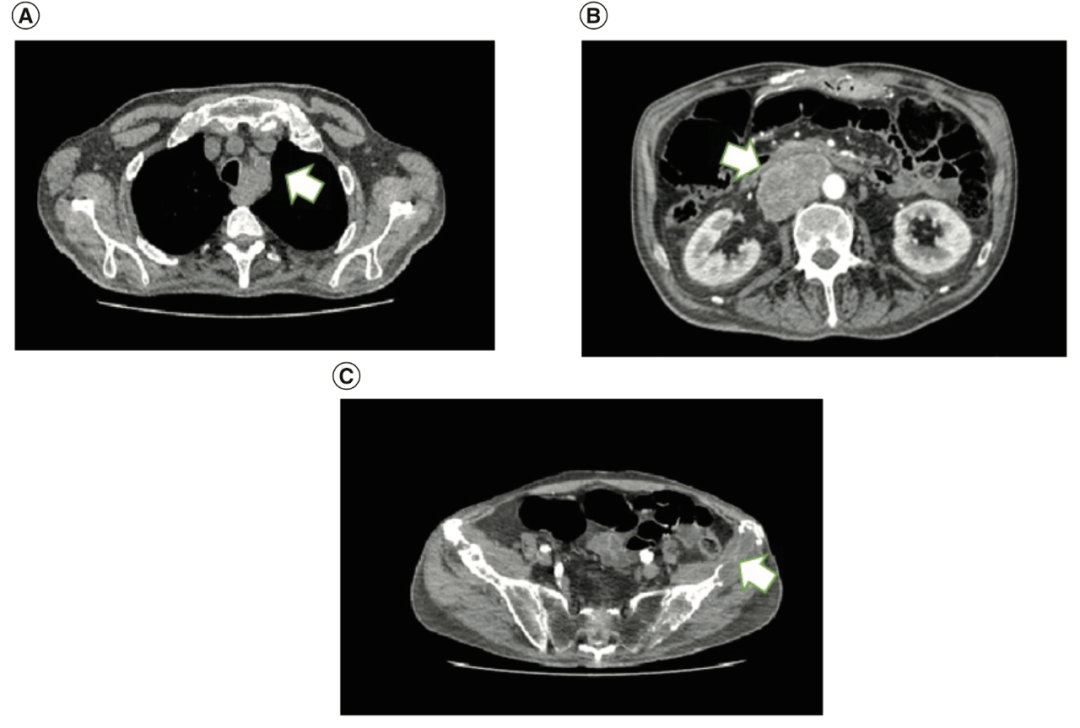
图 1 患者接受纳武利尤单抗治疗前 CT 显示(A)纵隔、(B)腹膜后和(C)骨转移灶。
但是 5 个周期后,患者因骨盆和腹部疼痛、体重下降、气急等不适至医院就诊,PS 评分为 2 分。患者再次行全身 CT 检查,颈部纵隔淋巴结较前明显增大,最长径约 60 mm,压迫食管和气管侧向偏移。腹部肿块大小约 82*48 mm,侵犯右肾动脉、腹主动脉右侧和十二指肠水平部。左髂骨翼部可见一病理性骨折,左侧肾上腺见一直径为 22 mm 的转移灶(图 2)。
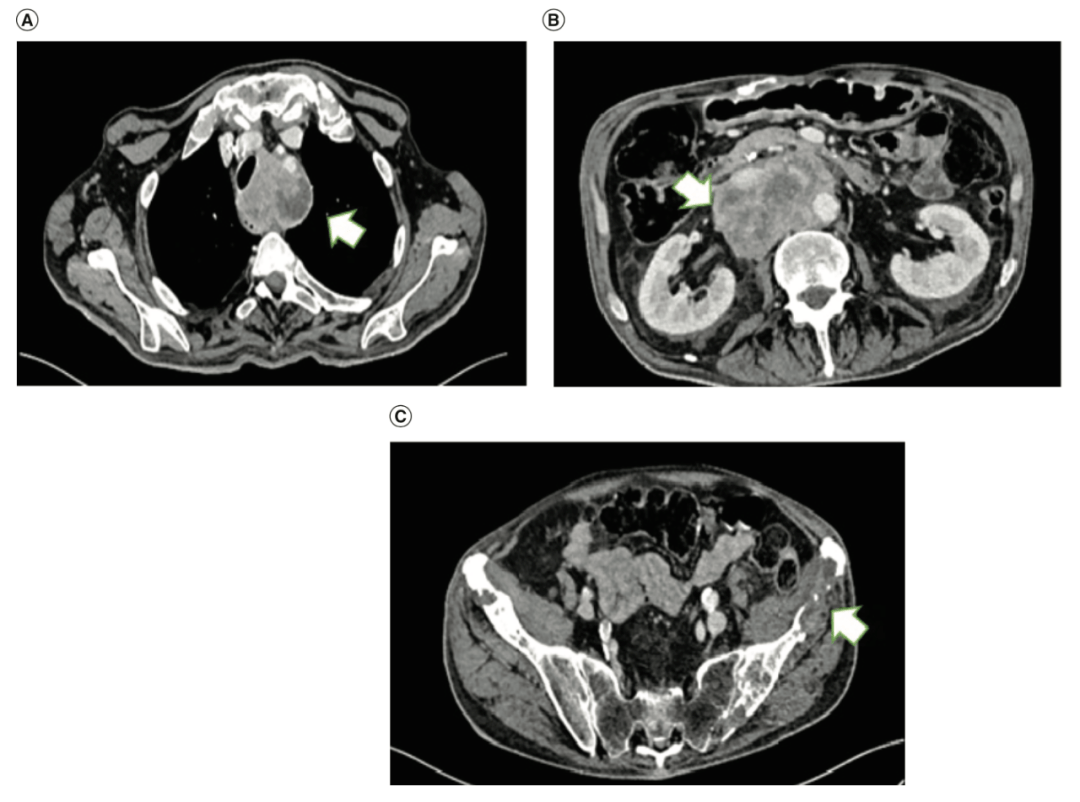
图 2 患者接受五周期纳武利尤单抗治疗后 CT 显示(A)纵隔、(B)腹部和(C)骨转移灶。
血常规提示血红蛋白 8.5 g/dl,中性粒细胞 6.92*10^9/L,淋巴细胞 0.99*10^9/L,血小板 850*10^9/L /ul,中性粒细胞/淋巴细胞比例为 6.98,血小板/淋巴细胞比例为 858,血清铁蛋白 1200ug/L,C 反应蛋白为 55 mg/L,显示患者为明显的炎症状态。患者接受纵隔巨大淋巴结 VMAT 放疗(3 Gy*10),并继续接受纳武利尤单抗免疫治疗。
放疗过程中,患者气急以及骨和腹部疼痛迅速得到缓解、体重逐步增加、PS 评分改善、运动功能恢复。放疗结束后 30 天,患者全身 CT 显示纵隔淋巴结转移灶缩小至 33*29 mm、左侧肾上腺转移灶缩小至 9 mm、腹腔转移灶缩小至 44*19 mm(图 3)。实验室检查显示血红蛋白上升至 12.9 g/dl,中性粒细胞 2.75*10^9/L,淋巴细胞 1.47*10^9/L,血小板 473**10^9/L, 中性粒细胞/淋巴细胞比例为 1.81,血小板/淋巴细胞比例为 292,血清铁蛋白 400ug/L,C 反应蛋白为 5 mg/L。放疗联合免疫治疗使患者全身炎症反应状态明显减轻。截至 2022 年 5 月,患者仍继续接受纳武利尤单抗免疫治疗,累计已接受纳武利尤单抗 32 周期,患者耐受性良好,疾病得到了控制,生化指标在正常参考范围内。
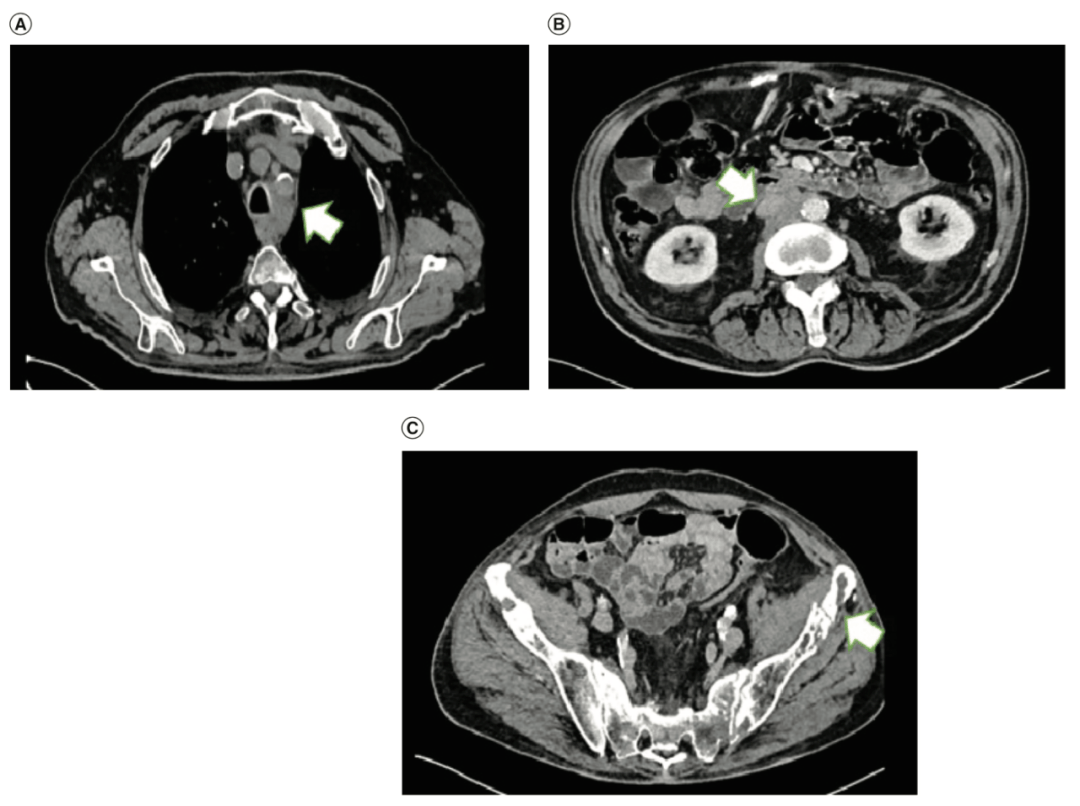
图 3 纵隔淋巴结转移灶姑息放疗结束后 30 天 CT 显示(A)纵隔、(B)腹部和(C)骨转移灶明显退缩。
归纳总结
该患者被诊断为喉癌虽然是不幸的,但是患者在接受标准的全喉切除术、颈部淋巴结清扫术以及辅助放疗后,得到了较长的无疾病生存期 (DFS)。
虽然在 5 年左右出现了局部复发和转移、标准一线双药含铂方案联合西妥昔单抗效果欠佳、无疾病进展期(PFS)仅 5 个月、二线单药纳武利尤单抗出现了超进展,但是在纵隔淋巴结转移灶局部姑息放疗并继续纳武利尤单抗免疫治疗后,患者的症状得到了迅速缓解,骨转移灶及其他转移灶均出现了明显缩小的远隔效应,截止末次随访时,患者的 PFS 已达 2 年余。
本文作者认为,该患者能取得如此明显的「远隔效应」的原因之一可能在于患者主要表现为淋巴结转移,对转移的淋巴结进行放疗可能能有效的触发肿瘤新抗原的释放,使「冷肿瘤」转化为「热肿瘤」,从而增强先前的免疫治疗疗效。
通过个体化的放疗联合免疫治疗来诱发「远隔效应」可能是未来解决转移性头颈部鳞癌的一个方法。
审核专家:
专家点评:
对于肿瘤的放射治疗,属于局部的治疗,而对于伴有转移的局部晚期或晚期肿瘤来说,主要治疗模式是内科系统治疗。然而,对于系统治疗来说,不管是化疗、靶向、甚至是肿瘤免疫治疗,都不可避免会出现耐药问题,那么,如何把放疗等局部治疗融入肿瘤的整体治疗策略,从而提高全身治疗的效果,是值得我们探索的研究方向。
在该案例中,结合以前的文献学习,我们认识到,对于放疗的远隔效应来说,如果没有联合免疫治疗,单纯局部放疗的远隔效应是很罕见的;然而,当放疗联合全身免疫治疗的时候,对于部分晚期肿瘤患者,可能会出现放疗后远隔效应,从而延缓或克服免疫治疗耐药问题,也就是就会有 1+1>2 的效应。
尽管在既往的文献报道中,当放疗联合 PD-1 单抗等免疫治疗时,远隔效应发生率大概约 20%。然而,仍有一些需要明确的问题:第一,放疗后远隔效应,目前主要还是小样本,或个案报道,并不具有普遍性,放疗与免疫联合的疗效,需要进一步临床研究的证实;第二,放疗联合免疫治疗的策略,也是需要进一步优化和探索;第三,放疗联合免疫治疗潜在获益人群的疗效预测标志物,需要进一步明确和探索。
作者:小壮壮;审核:齐晓光
排版:景胜杰;题图:站酷海洛
投稿:jingshengjie@dxy.cn
参考文献
1. Hwang WL, Pike LRG, Royce TJ, et al. Safety of combining radiotherapy with immune-checkpoint inhibition. Nat Rev Clin Oncol. 2018;15(8):477-494.
2. Liu Y, Dong Y, Kong L, et al. Abscopal effect of radiotherapy combined with immune checkpoint inhibitors. J Hematol Oncol. 2018;11(1):104.
3. Marco F, Gianluca A, Mariagrazia T, et al. Overcoming immune-resistance in laryngeal cancer: a case report of the abscopal effect and nivolumab beyond progression. Immunotherapy. 2022;14(14):1089-1095.返回搜狐,查看更多

