“艺术”两字在CSCO-赛诺菲胸部肿瘤及血液移植高峰论坛的血液移植分会场中被提及不下10余次,如何让造血干细胞移植从“技术”跃升为“艺术”层面,血液移植专家们的经验之道你不可错过!
作者丨希捷
来源丨医学界肿瘤频道
3 月 11 日, 由中国临床肿瘤学会(CSCO),北京希思科临床肿瘤学研究基金会与赛诺菲公司联合举办的“肿瘤治疗艺术·CSCO赛诺菲胸部肿瘤及血液移植高峰论坛”在上海隆重召开。
在主论坛和血液移植分会场上,国内知名学者分享了血液肿瘤领域的“中国好声音”,同时深入探讨了优化造血干细胞移植(HSCT)的策略,为移植从技术跃升为艺术指明了方向。
回顾血液肿瘤领域的“中国声音”

黄晓军教授
北京大学人民医院、北京大学血液病研究所黄晓军教授回顾了中国在血液恶性肿瘤治疗中取得的原创成果。急性早幼粒细胞白血病(APL)曾是一种极为凶险,死亡率很高的恶性血液疾病。
上海交通大学医学院附属瑞金医院、上海血液学研究所陈竺院士团队应用全反式维甲酸(ATRA)和三氧化二砷(ATO)对 APL 进行联合靶向治疗,使得该病的5年无病生存率跃升至90%以上,达到基本“治愈”标准。同时,他们从分子机制上揭示了 ATRA 和砷剂是如何分别作用于 APL 致病分子 PML/RARα,将白血病细胞诱导分化和凋亡,从而达到疾病治疗的目的。
“上海方案”是一项真正的结合临床医学与基础生物学的研究,是东方传统医学和西方医学结合的典范,开启了在恶性血液疾病中转化治疗的重要篇章。领衔该方案的陈竺院士也因此在 2016 年获得了美国血液学会(ASH)颁发的“欧尼斯特·博特勒奖”。
与“上海方案”交相辉映的是国际原创的单倍型相合移植系“北京方案”,其令单倍型移植达到了与同胞相合移植的同等疗效,使全球 HSCT 进入了“人人都有供者”的新时代。
“北京方案”中创新应用粒细胞集落刺激因子(G-CFS)诱导免疫耐受并联合抗胸腺细胞球蛋白(ATG)的研究为单倍型移植成果奠定了基础,突破了欧美研究者眼中的“禁区”,北京大学人民医院黄晓军教授也因此获得了“欧洲骨髓移植协会圣安东尼成就奖”和“国际恶性血液病大会杰出贡献奖”。
“北京方案”改变了全球 HSCT 的格局,获得了国际同行的认可(图1),该方案的广泛应用使全球 HSCT 进入快速发展期。

图1 “北京方案”获得国际同行认可
在北京大学人民医院、北京大学造血干细胞研究所刘开彦教授介绍的 2007-2016 造血干细胞移植现状中,我们能清晰地看到我国 HSCT 总例数、异基因移植和自体移植总例数均在不断增长。就中美数据对比而言,半相合和异基因移植在中国较为普遍,而自体移植在美国更多见,比例高达 54%。
随着“北京方案”的推广,半相合移植逐渐成为主流,在急性髓性白血病(AML)、急性淋巴细胞白血病(ALL)、骨髓增生异常综合征(MDS)和再生障碍性贫血(AA)等疾病的治疗中发挥越来越重要的作用。
对于慢性粒细胞白血病(CML)患者,由于酪氨酸激酶抑制剂(TKI)的应用,移植的占比逐年下降,但 HSCT 仍为急变和加速期患者带来明确获益。对于多发性骨髓瘤(MM)、非霍奇金淋巴瘤(NHL)和霍奇金淋巴瘤(HD)患者,自体移植仍是主要方式。
在回顾数据的最后,刘开彦教授还提出了一些值得关注的问题,如移植后复发的防治、老年患者的移植、移植后患者的综合管理等,这些问题需要通过严谨的临床研究进行探索,也需要在条件成熟时形成共识或指南类的指导性文件。

刘开彦教授
优化供体选择:从“人人”到“最佳”
供者匮乏制约了 HSCT 的开展,在中国学者的不懈探索下,“人人都有移植供者”的梦想基本实现,单倍型供者的比例不断攀升。但问题又来了,如何选择最佳的移植供者,从而达到最好的治疗效果?苏州大学附属第一医院、江苏省血液研究所陈苏宁教授和北京大学人民医院的常英军教授对此从基础和临床两方面给予了解答。
基础进展

陈苏宁教授
陈苏宁教授指出,HLA 基因是影响移植预后最重要的因素之一,多数研究认为 HLA-A,B,C 及 DRB1 位点不合与临床预后密切相关,存在上述位点中的不合时,会有更高的移植物抗宿主病(GVHD)及死亡风险。
对非血缘移植受者型筛选HLA相匹配供者时,至少需对 HLA-A, -B, -C, -DRB1, -DQB1 这几个位点进行供受者高分辨配型,尽量避免>1 个位点不合的供者。当有 2 个或 2 个以上 10/10 全合的非血缘供者时,则建议优选 ABO 血型及 DPB1 相合的供者,同时在已致敏受者中,需要检测供者特异性抗体(DSA)。
此外,特定位点不合对临床结局的影响可能随着原发病类型、GVHD 预防方案(去T或不去T)及预处理方案的不同而发生变化。新一代基因测序技术(NGS)的发展可对HLA基因全长(包括内含子)进行高分辨测序,目前其正快速进入到临床HLA配型实验室,用于非血缘供者的筛选有不少优势。
除HLA基因外,包括次要组织相容性抗原基因、NOD2 基因型、KIR 基因型、TLR9 基因、IL-10 基因等非 HLA 基因型也被发现可能对预后产生影响。
临床进展

常英军教授
常英军教授指出,首先是要明确不同供者移植在花费、GVHD、感染、复发风险等方面存在差异,虽然单倍型供者易获得,但也存在高感染等缺点(表1),因此在单倍型相合移植时代,仍要把握供者选择的基本原则(图2)。
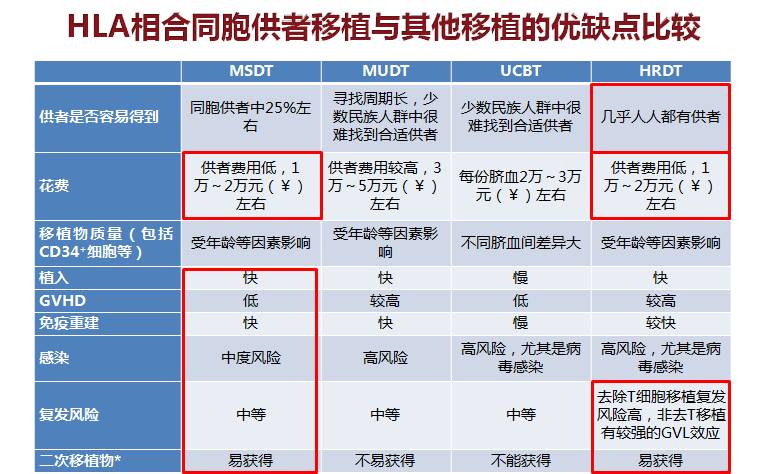
表1 不同供者移植方案的优缺点
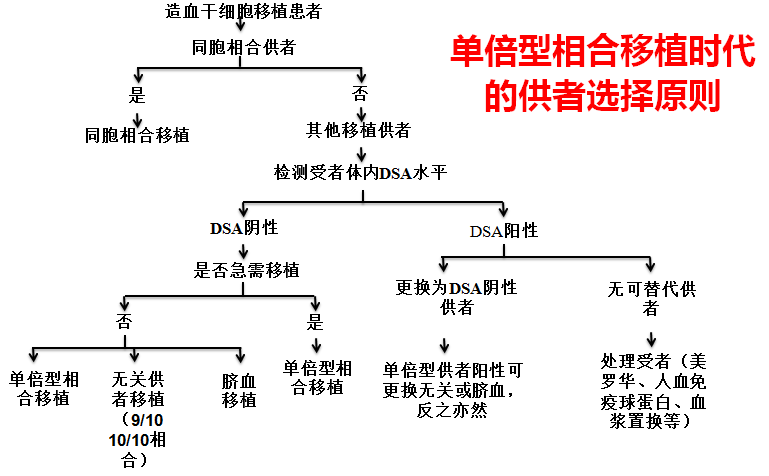
图2 单倍型相合移植时代的供者选择原则
把握基本原则之后,为了在“为数不少”的潜在供者中选择最佳人选,还需考虑到 DSA、供者年龄和性别、供受者关系、非遗传的来自母亲的抗原(NIMA)错配等一系列情况,可参考以下原则(图3)。

图3 更为细化的单倍型相合移植的供者选择原则
当然,遵循上述原则能解决移植供者选择的部分问题,但常教授仍提醒道,“影响预后的因素因半相合移植模式不同而异,选择供者时应考虑到移植模式,应用发展的眼光看待供者选择原则且不断更新,并兼顾每个中心的具体情况。”
优化预处理方案:加入ATG获益明确
成功的 HSCT 离不开完善的预处理,预处理的价值不仅在于抑制并功能性清除受体的免疫系统,使供者干细胞得以归巢而不被排斥,而且还能清除原发恶性肿瘤,或将白血病细胞长期控制在最小范围,同时产移植物抗白血病效应(GVL)。第三军医大学新桥医院张曦教授介绍了如何运筹帷幄,才能让造血干细胞移植预处理展现“魔力”。

张曦教授
三类预处理方案各有特点
三大类预处理方案--清髓(MA)、非清髓(NMA)和减低强度(RIC)各有特点。MA 的优势在于清除原发恶性肿瘤快速而强烈,缺点在于骨髓毒性强,移植相关死亡率(TRM)高、cGVHD 发生率高;NMA 能改进 MA 的缺点,它细胞清除量和骨髓毒性最小,主要依赖移植后的 GVL 效应来清除原发病,多用于无法耐受MA的老年患者。RIC 介于 MA 与 NMA 之间,其优点在于急性毒性降低,适用于老年及有合并症的患者,有助于降低死亡率,代价则是牺牲部分放化疗的抗肿瘤效应。
合理选择预处理方案
中国学者研究证实,G-CSF 预激预处理有助于降低高危AML患者复发率(图4)。此外,阿扎胞苷、氟达拉滨、索拉非尼在内的TKI等药物也被用于预防复发,效果不一而足。
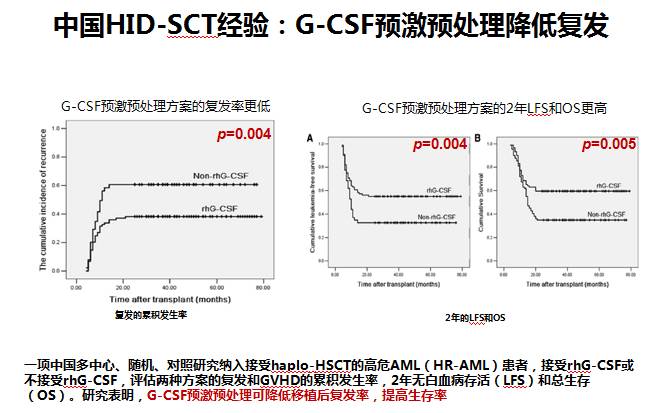
图4 G-CSF预激预处理可降低高危AML患者复发率
ATG有助于应对预处理介导的GVHD
体外研究显现抗白血病效应移植后的 GVHD 可谓是一个临床难题,虽然可以通过免疫抑制剂来应对,但可能面临复发率升高的风险。如何化解难题?研究者们不约而同地想到了抗胸腺细胞球蛋白(ATG)。早年曾有多项体外研究提示了该药具有抗白血病效应,2016 年发表的一项体外研究进一步提示 ATG 通过补体依赖及非依赖途径杀伤白血病细胞。
AML患者从ATG获益明确 2017 年发表的一项回顾性分析比较了 2006-2013 年首次接受 HLA 相同同种异体干细胞移植的AML患者,结果表明 RIC 预处理方案加入 ATG 能显著降低 cGVHD 发生率 [HR=0.16(0.31~0.48)],但复发风险未增加(图5)。无独有偶,对于 50 岁以上 AML 第一次缓解后给予 HLA 相合的同胞外周血干细胞移植患者,在 Bu/Flu 预处理方案中加入 ATG 后,cGVHD 发生率也得到下降(图6),更可喜的是,ATG 联合 CSA 组获得了更好的远期生存(图7)。
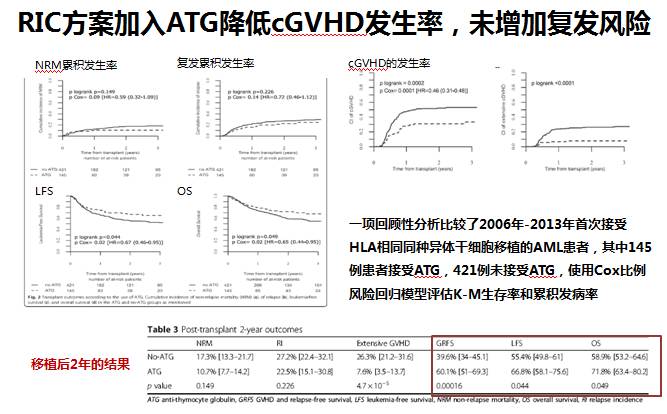
图5 RIC方案加入ATG未增加复发风险
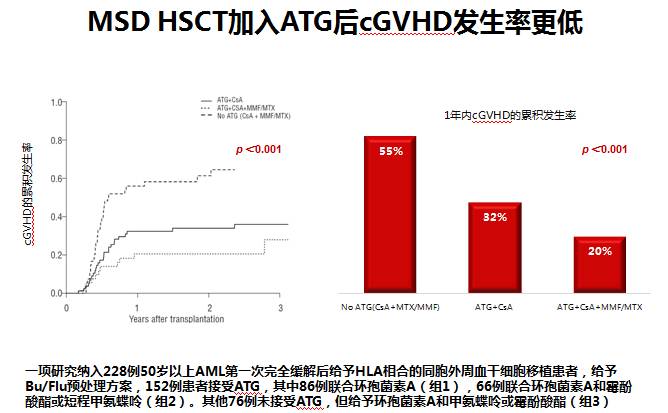
图6 加入ATG能显著降低cGVHD发生率

图7 ATG+CSA组患者获得更佳的远期生存
ATG获益进一步扩展ATG 在 AML 患者中的获益明确,在其他血液肿瘤患者中获益如何?2016 年发表在《柳叶刀·肿瘤学》的一项研究回答了这个问题。
这项多中心、Ⅲ期开放标签、随机对照临床研究纳入符合条件的 16~70 岁患有血液恶性肿瘤和 Karnofsky≥60,接受 MA 或 NMA(或RIC)预处理方案,接受不相关供体造血细胞移植,1:1 随机在移植前予以 r-ATG 预防 GVHD 或标准预防 GVHD 方案,结果显示 ATG 能显著改善 cGVHD、无病生存期和生活质量评分(图8),且女供男、外周血供者、一个抗原或位点错配等亚组患者有更好的获益。
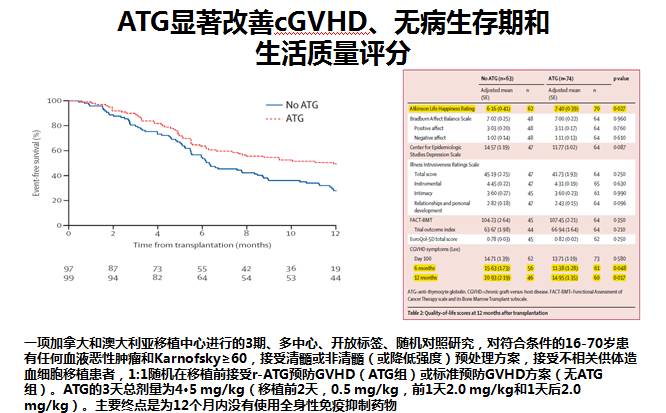
图8 ATG显著改善cGVHD、无病生存期和生活质量评分
优化移植后综合管理:减少复发和排异
一次完美的 HSCT 并不以移植结束而终止,复发和排异是移植后绕不过去的两道坎,甚至有学者提出了无复发/无排异生存(GRFS)来评价 HSCT 的结局,从而更精确地反映移植后的健康状态和更好的生活质量。如何应对复发和排异,让移植成果得以保存,上海交通大学医学院附属瑞金医院胡炯教授分享了这方面的经验。

胡炯教授
移植后复发的管理
监测移植后复发分为血液学、细胞遗传学和分子生物学复发三种,后者是当前研究的热点。检测微小残留病变(MRD)能反映分子生物学复发,有助于选择高危患者和制定个体化治疗方案,从而提高生存率。2016 年美国血液学年会上有学者报道了通过二代测序联合流式来检测 MRD,可能成为今后新的趋势。
预防和治疗方式包括减停免疫抑制剂、预防性供者淋巴细胞输注(DLI)、应用靶向治疗药物(如伊马替尼等)、使用肿瘤疫苗等。对于出现复发的患者,可以采用靶向药物TKI进行抢先治疗,当然也可以尝试改良 DLI 或 IFN-α 治疗。近年来,嵌合抗原受体T细胞(CAR-T)治疗 B 细胞恶性肿瘤 allo-HSCT 后患者显示出一定效果,低甲基化药物维持治疗也成为了潜在选择。
移植后GVHD的控制由于 aGVHD 中供体T细胞仍是主要机制,所以清除或抑制T细胞是预防 GVHD 的最有效途径。近期发表的一项荟萃分析显示,ATG 用于 GVHD 预防有明显优势,且对复发无明显影响(图9)。对于 cGVHD 的一线系统治疗,需要持续调整免疫抑制剂,过度治疗和疗效不足都应避免。目前 cGVHD 二线治疗尚未达成共识,主要依靠医生经验、基于药物治疗反应率、临床监控、毒性风险和基础疾病复发风险等因素。当然,对于 GVHD 必须牢记“重在预防”!
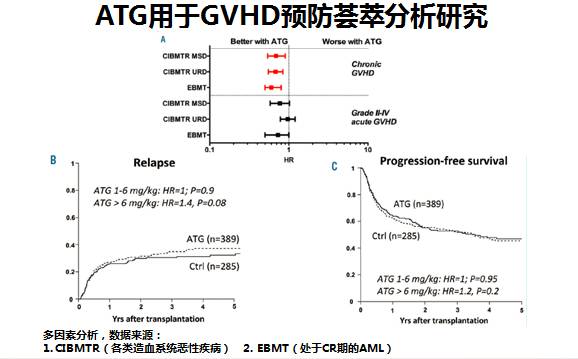
图9 荟萃分析显示ATG用于GVHD预防有明显优势
除外复发和排异,HSCT 的长期并发症也不容忽视(表2),同样需要予以关注。
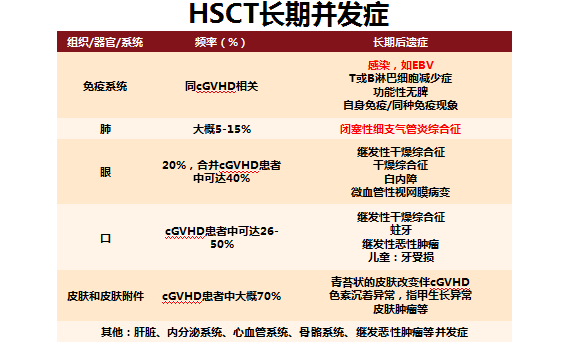
表2 HSCT长期并发症与发生率
从技术到艺术,从数量到质量
刘开彦教授在会议总结中指出,造血干细胞移植是“艺术”,艺术需要灵感,其复杂之处在于无法生搬硬套教科书,而是要依靠临床经验在降低复发风险与减少 GVHD 之间寻求平衡点。
造血干细胞移植疗效的不断改善需要综合考虑包括供者选择、移植预处理、移植后综合管理等因素,只有这样做才能将中国病例数量的优势实实在在地转化为治疗水准的提高,让移植艺术得以展现,助力生命之完美。
讨论环节掠影

第一部分讨论环节主持人吴德沛教授与嘉宾合影(从左至右为常英军教授、胡建达教授、李军民教授、吴德沛教授、王椿教授、任汉云教授、江明教授)

第二部分讨论环节由黄河教授主持

第二部分讨论环节嘉宾合影(从左至右分别为胡炯教授、罗依教授、常英军教授、徐雅靖教授、赖永榕教授、唐晓文教授、王顺清教授、张曦教授)

参会专家现场提问
SACN.ONC.17.02.0483y
(本文为医学界肿瘤频道原创文章,转载需经授权并标明作者和来源。)