
什么是“中间期肌无力综合征”?带你认识。
作者|张盛 台州市第一人民医院
来源|医学界神经病学频道
肌无力症是由神经肌肉传递障碍所导致的一系列临床症状群。在神经内科,大家首先想到的神经肌肉接头障碍性疾病肯定是重症肌无力,但若是一个渐进性的病程,就应该考虑中毒、代谢、遗传或肿瘤等因素。今天与大家分享的就是由有机磷农药中毒引起的“中间期”肌无力综合征。
一、什么是“中间期”肌无力综合征?
这种综合征从时间逻辑上来讲跟神经外科的硬膜外血肿引起的中间清醒期有点类似,中间期肌无力综合征(intermediate myasthenia syndrome,IMS)又叫中间型综合征(intermediate syndrome,IMS)是指在急性有机磷中毒(acute organophosphorus pesticide poisoning,AOPP)后1~4 d,经过治疗急性胆碱能危象已经消失,迟发性神经病变出现之前,部分患者出现的以颅神经支配的肌肉、四肢近端肌肉、屈颈肌以及呼吸肌无力或麻痹为特征的一组临床表现,发生率为5.4%~13.8%。重症患者可因呼吸肌麻痹致呼吸衰竭而死亡,病死率为23.5%~42.6%。
二、有机磷中毒后为什么会出现IMS?
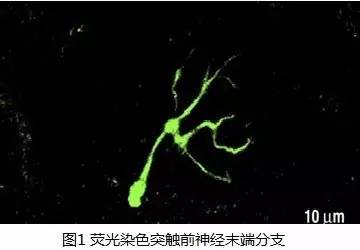
首先让我们来回顾一下肌肉收缩的神经传导过程:神经肌肉接头由突触前轴突终端(如图1)和突触后肌端板(如图2)组成,在突触前终端囊泡中含有乙酰胆碱(神经递质),这些囊泡中的蛋白质被称为突触蛋白结合肌动蛋白细胞骨架。当神经冲动到达末稍时,动作电位诱导的钙离子通道开放,细胞内钙离子浓度增加促进突触蛋白磷酸化,这种磷酸化导致细胞骨架中的乙酰胆碱释放,乙酰胆碱从突触前膜释放后进入突触间隙,和突触后膜上的乙酰胆碱受体(AchR)结合,导致细胞膜兴奋,钠离子内流,膜电位转变为外负内正,骨骼肌细胞发生兴奋而收缩。
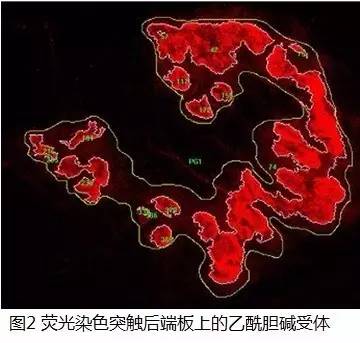
*图2 乙酰胆碱受体分布在突触后膜端板的褶皱交界处,电压门控Na +通道也主要集中在褶皱处。乙酰胆碱受体可与一定数量的乙酰胆碱可逆性地结合。当它们结合在一起时,受体离子通道被打开,Na+内流,伴随一个快速的去极化过程。如果这个终端电势足够大,就会使肌肉纤维产生动作电位,从而引起肌肉收缩。随后在突触中的乙酰胆碱被胆碱酯酶迅速分解,从而使肌肉复极化。
在有机磷中毒急性期,由于对胆碱酯酶的抑制作用,使得横纹肌-肌内接头处乙酰胆碱蓄积,从而导致横纹肌持续收缩,临床上可表现为面、眼、舌、四肢、全身的肌束震颤,被称为N样症状(烟碱样症状)。既然有N样的症状表现,又怎么会引起肌无力的情况呢?
到目前为止,有机磷类毒物对神经肌接头的影响机制还不是完全清楚。
● Wecker, L等人发现,选择性地使用丁酰胆碱酯酶(一种能与大部分有机磷结合的胆碱酯酶血浆蛋白)抑制剂对肌无力的发展没有影响,而通过使用氯解磷定重新激活乙酰胆碱酯酶(AChE)能预防肌无力的发生,进一步证实了只有乙酰胆碱酯酶抑制剂才会导致肌无力的发生;同时在离体的啮齿动物肌肉中使用AChE抑制剂可以导致肌肉坏死,表现为运动终板区的线粒体扩张,肌浆网改变,突触褶皱形态的变化。
● Maselli等人的研究表明,神经肌肉接头在接触乙酰胆碱酯酶抑制剂后端板的受体由于受到持续性去极化影响,其灵敏度的下降并导致神经肌肉传递失败。既往对IMS患者的重频神经刺激肌电图(repetitive nerve stimulation electromyography,RNS)和电刺激单肌纤维肌电图(stimulation single fiber electromyography,SSFEMG)的研究结果亦表明,神经肌接头突触后传导阻滞是其肌无力发生的主要机制。
● 也有学者推测,有机磷中毒后引起的氧自由基直接损伤肌肉从而引起肌无力。
综上所述,IMS可能是一种由有机磷中毒引起的神经功能失调、神经肌肉传导阻滞、肌肉损伤共同参与的神经性麻痹综合征。
三、如何诊断IMS?
1.明确的有机磷类药物接触史。
2.参照 《职业性急性有机磷农药中毒的诊断及处理原则》(GB7794-87)确诊为重度或中度急性有机磷中毒者,全血胆碱酯酶活力持续降低。
3.经过救治后胆碱能危象基本控制,于急性中毒后1~4d左右出现以肌无力为特征的临床表现,肌无力可累及部分颅神经支配的肌肉、屈颈肌及四肢近端肌肉、呼吸肌这3组肌肉或其中2组肌肉,且肢体肌力降至或低于3级者;腱反射可普遍低下,无感觉障碍,一般无上运动神经元损害的表现(不包括继发于缺氧后出现病理反射者)。
4.临床出现肌无力时,高频重复刺激周围神经的肌电图检查可见诱发肌肉复合电位的波幅递减,呈现类似重症肌无力的肌电表现(如图3);血淋巴细胞乙酰胆碱烟碱受体(nAChR)特异结合活性增高。
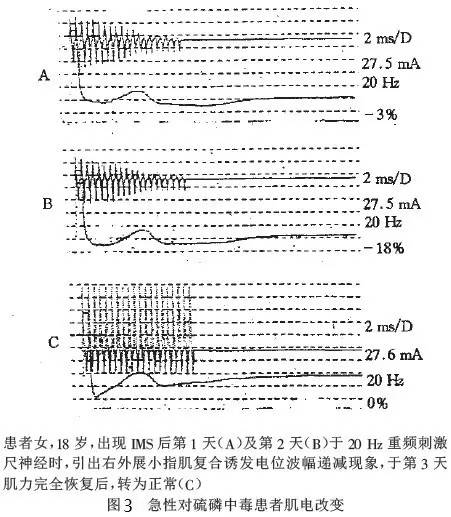
5.排除急性有机磷中毒“反跳”所致的中枢性或周围性呼吸衰竭、有机磷中毒引起的迟发性多发性神经病、格林-巴利综合征、重症肌无力胆碱能危象、低血钾症等。
四、IMS的分级标准?
轻型:出现屈颈肌、四肢近端肌肉无力和(或)部分颅神经支配的肌肉无力。
重型:出现呼吸肌麻痹和(或)因第IX及第X对颅神经支配肌肉的无力引起上气道通气障碍者,可伴有或不伴有轻度IMS的有关表现。
五、发生IMS的高危因素和持续时间?
IMS是急性有机磷农药神经毒性作用所致的临床综合征之一,王均招等人在分析了226例急性有机磷中毒患者的临床资料后得出:IMS组与非IMS组的中毒农药种类、中毒量、有无抬头困难、肌颤、使用复能剂、血白细胞数、血钾、PaCO2、PaO2比较,差异有统计学意义;同时两组性别、年龄、中毒途径、中毒至开始救治时间、人院时的中毒程度、中毒后有无出汗、流涎、呕吐、腹痛、腹泻,有无基础并发症、首次胆碱酯酶测定值、pH值、达阿托品化时间及病死率比较,差异均无统计学意义。
通过多元Logistic回归分析共筛选出3个IMS的独立危险因素:分别为中毒后出现抬头困难、急性期血白细胞增高、PaCO2增高。在出现呼吸肌麻痹前,都已有屈颈肌及四肢近端肌力和(或)颅神经支配肌力的减退,因此临床诊疗过程中必须高度重视患者乏力的主诉,及时作相关肌力检查。临床工作中抬头困难是一个比较容易确认的体征,检查时,以平卧患者后枕部能否自主抬离床面为准。若不能轻易完成,肯定存在肌无力;勉强完成抬头,但不能独立由平卧位坐立,也表明存在肌无力。
仅有屈颈肌、肢体近端肌肉或颅神经支配肌肉无力的轻型IMS患者,多于2~4d后缓解或恢复。而出现呼吸肌麻痹并兼有上述肌肉无力的重型IMS患者,经及时机械通气及支持治疗,多于10~23d后恢复自主呼吸。以颅神经支配的肌肉肌力最早恢复,其次是屈颈肌,而呼吸肌和肢体肌力恢复较晚。
六、IMS的治疗原则?
在治疗急性有机磷中毒的基础上,根据IMS的病情不同采用以下治疗:
1.轻 型IMS:本型有较高的自限性,主要为对症处理,保证热量供应及电解质平衡。但应密切观察病情,警惕和防备向重型进展。
2.重 型IMS:对出现胸闷憋气、咳嗽无力、轻度呼吸困难的患者给予吸氧,吸氧不能缓解的重度呼吸困难者,或表现呼吸浅快微弱,胸部呼吸动度减低,双肺呼吸音低,唇、甲发绀,心率加快、多汗,继而出现意识障碍时,应及时建立人工气道给人工通气,加强呼吸道护理,防治并发症,直至呼吸肌无力完全恢复。
七、IMS的预防?
洗胃彻底及时是抢救AOPP的首要措施之一,若洗胃不彻底,部分毒物滞留胃内或进入肠腔被重复吸收,可致IMS发病率增高;同时AOPP患者使用阿托品后有明显“阿托品化”表现者很少发生IMS,而“阿托品化“表现不明显者,阿托品用量难以把握,IMS发生率高。故在临床诊疗过程中需掌握有效的洗胃方法,及维持阿托品化至胆碱酯酶活力稳定在正常值50~60%以上,才能有效减少或防止IMS的发生。
八、IMS的预后?
既往研究报道,出现IMS会导致死亡率上升,但随着机械通气支持技术的普及,只要做到早期诊断、早期正确运用呼吸机支持技术,IMS并不会增加AOPP的病死率。且IMS有很高的自限性,肌无力状态一般在4~18 d后完全恢复正常。但在这类病人中特别需要警惕:尽管部分患者行经口气管插管治疗后达到撤机拔管标准,往往拔管后可能再次出现呼吸衰竭的表现!且需要再次建立人工气道!这是因为IMS患者在呼吸肌无力的同时,存在第Ⅸ、X对颅神经支配肌肉的无力,咽喉部肌肉麻痹可导致上气道通气障碍及呼吸困难。
有报道认为颅神经支配肌肉肌力恢复较呼吸肌为先,但呼吸肌强度恢复到正常的50%即可维持通气基本的需要,而此时呼吸肌耐力差,易疲劳,咽喉部肌肉麻痹又尚未完全恢复,气管捕管导致上呼吸道黏膜水肿,拔管后气道阻力明显增加,故在监护中患者很快出现呼吸肌疲劳,并需要再次开放气道行呼吸支持。对待此类患者预计长时间机械通气必要时可行气管切开,因为气管切开去除了占总气道阻力75%的上呼吸道阻力,减少了IMS患者呼吸肌需要做的功,避免了未完全恢复的咽喉部肌群和上呼吸道黏膜水肿增加的阻力,有利于其肌力的恢复和长久的保持。
参考文献
[1]Kumar GC, Bhuvana K, Venkatarathnamma PN, Sarala N. Serum creatine phosphokinase as predictor of intermediate syndrome in organophosphorus poisoning. Indian J Crit Care Med. 2015. 19(7): 384-7.
[2]Bird SB, Krajacic P, Sawamoto K, Bunya N, Loro E, Khurana TS. Pharmacotherapy to protect the neuromuscular junction after acute organophosphorus pesticide poisoning. Ann N Y Acad Sci. 2016. 1374(1): 86-93.
[3]Karami-Mohajeri S, Nikfar S, Abdollahi M. A systematic review on the nerve-muscle electrophysiology in human organophosphorus pesticide exposure. Hum Exp Toxicol. 2014. 33(1): 92-102.
[4]Karalliedde L, Baker D, Marrs TC. Organophosphate-induced intermediate syndrome: aetiology and relationships with myopathy. Toxicol Rev. 2006. 25(1): 1-14.
[5]王均招, 陈伟庆, 王琥. 急性有机磷农药中毒中间综合征的危险因素分析. 中华劳动卫生职业病杂志. 2006. 24(6): 369-370.
[6]秦复康, 何凤生, 刘统俊等. 急性有机磷农药中毒"中间期肌无力综合征"的诊断及分级诊断. 中华劳动卫生职业病杂志. 2000. 18(3): 146-150.
[7]肖诚, 杨东仁, 牛勇, 秦复康, 何凤生. 急性有机磷农药及其混剂中毒患者单肌纤维肌电图的研究. 中华劳动卫生职业病杂志. 2001. 19(4): 257-260.
[8]陈军, 林爱华, 庄红. 不同气道开放方式对急性有机磷农药中毒重型中间综合征的应用. 中华劳动卫生职业病杂志. 2009. 27(4): 231-232.