作者:解螺旋.翠花 解螺旋原创
转载请注明来源:解螺旋,医生科研助手
有人开玩笑说,人是细菌制造出来的宇宙飞船,有了这个飞船,细菌就远远扩大了它们的活动范围,小伙伴们有没有感觉很有道理?今天翠花就和大家一起聊聊在人类的肠道中存在着大量以细菌为主的微生物,看看它们是如何机智的在“飞船”中繁衍生息的(如何与人体免疫息息相关)。
据估计,正常成人体内的肠道细菌总重量可达1-1.5公斤,包含的细菌数量可达1014个。这个数字大约是人体全部细胞的10倍。历经长期进化,这些细菌跟宿主之间建立了稳定的共生关系。我们为其提供食物和居所,它们为我们的消化系统和免疫系统提供支持。正常生理状态下,肠道细菌可以促进宿主免疫系统的发育,并可通过脂多糖、脂蛋白以及代谢产物等特定组分调控宿主的免疫反应,形成一道肠道生物屏障。

图片来源Nature杂志. doi:10.1038/4441009a
肠道微生物对宿主免疫系统的影响受到越来越多的关注。10月8日出版的最新一期Cell杂志,刊登了两篇背靠背文章,讲述了肠道细菌对免疫细胞的调节。这些很特别的细菌非常“黏人”,粘附在肠道上皮上,诱导了Th17免疫细胞的激活。
第一篇文章介绍了三类细菌,都是通过先跟肠道上皮细胞发生粘附再激活Th17。Th17细胞是辅助性T细胞,因分泌白介素17(interleukin 17, IL-17)而得名。在自身免疫性疾病和机体防御反应中具有重要的意义。

(一) “土著”细菌:分节丝状菌(SFB)
SFB广泛存在于人或多种脊椎动物肠道内。首先观察到SFB特异性的粘附在小肠上皮上,粘附性质具有种属特异性。


接着,用RNA-seq手段检测了SFB粘附到小肠上皮细胞,对小鼠的遗传背景产生的影响,在被粘附的上皮细胞中检测到了以下分子表达上调:
血清淀粉样蛋白(SAA)
胰岛再生源蛋白(Reg3β和Reg 3γ)
一氧化氮合酶(NOS2)
双功能氧化酶(DUOX2,促进活性氧ROS生成的酶)
双氧化酶成熟因子(DUOXA2)
(二) 胞外致病菌
这里选了柠檬酸杆菌(C.rodentium),它跟SFB不同,定殖在小鼠肠道的结肠部位。同样RNA-seq检测结肠上皮细胞的转录组的变化,发现上调的基因跟上面提到的基因部分重叠,包括:DUOX2、DUOXA2、RegIIIb、RegIIIg和NOS2。
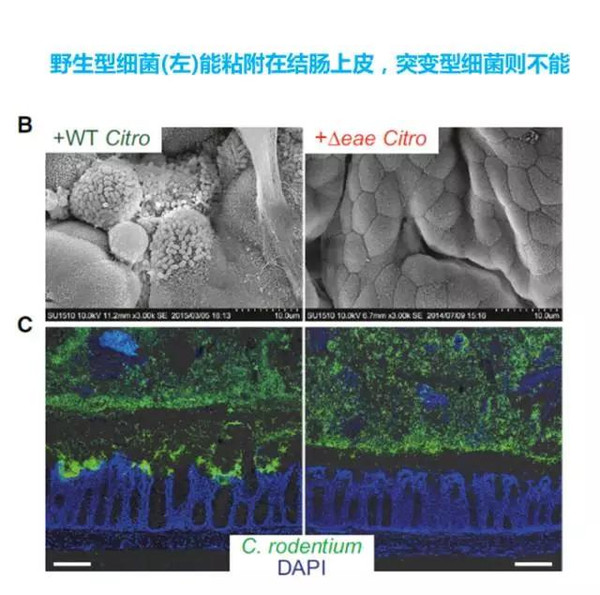
(三) 从人粪便分离的20株细菌
通过基因组测序对分离的20种细菌的种属做了鉴定。与SFB具有种属特异性不同, 人类分离的细菌既能定殖到小鼠肠道上皮也能定殖到大鼠肠道上皮,被粘附的上皮细胞中NOS2和DUOXA2表达上调,3型天然淋巴细胞(ILC3)和 IgA应答,Th17激活。且不产生炎症反应,可能在临床上有一定的应用价值。
这里选择了另外17株梭状芽胞杆菌作为对照,平行实验发现,这些菌不能粘附在上皮细胞表面,也无法激活Th17细胞。文献报道这17株菌能够诱导另外一种T细胞(Treg细胞)的激活。说明了粘附对于Th17细胞的激活是必须的。

第二篇只用了一种微生物SFB作为候选细菌,同样证实了该细菌能粘附于小肠上皮细胞,并诱导Th17细胞激活。

但这篇文章重点在于分析SFB诱导Th17细胞分泌IL-17的机制。跟第一篇文章一样,都关注到了细菌粘附的上皮细胞中基因表达谱的变化,并都找到了血清淀粉样蛋白(SAA),具体这个过程有以下几步:

同一期的Cell杂志发表了评论文章,对两篇文章的进行点评,同时给出了下面一张示意图,更形象的展示了细菌粘附下Th17细胞激活的过程。

图片来源Cell. 2015, 163(2):273-274.
总体来说,这两篇文章阐述了肠道上皮细胞对肠道微生物的新的响应方式和适应性免疫应答,突出了局部微环境对细胞因子产生的影响。虽然都没有把引起SAA分泌的细胞内信号转导过程和上游机制讲清楚,但这个现象的发现对未来将Th17细胞应用于控制局部致病感染和全身性自身免疫反应有重要的意义。
参考文献:
Atarashi et al., 2015, Cell 163, 1-14
Sano et al., 2015, Cell 163, 1-13
https://dx.doi.org/10.1016/j.cell.2015.09.040

 )
)






























我来说两句排行榜