导读: 双(多)特异抗体(BsAb)是含有两种(多种)特异性抗原结合位点的人工抗体,能在靶细胞和功能分子(细胞)之间架起桥梁,激发具有导向性的免疫反应,在肿瘤等疾病治疗中表现出潜在价值。随着安进靶向CD19和CD3的双特异性抗体Blinatumomab的上市,极大地促进了双特异抗体的研发投入,现已成为抗体工程领域的一个热点。为满足发展需要,研发技术不断更新换代,CrossMAb技术也因此应运而生。
双特异IgG抗体产生中的主要挑战就是轻、重链的正确联结。以往最原始的方式是轻、重链随机联结成非对称的异源二聚体IgG抗体,会产生多种不需要的副产品;Knobs-into-holes(KiH)方法的使用解决了重链异二聚体的正确联结,但其类同的轻链的正确联结数十年来依然是个问题;而CrossMAb技术的出现保证了双特异性异二聚体IgG抗体中轻链的正确联结,它是基于双特异IgG抗体Fab臂功能域的交换而达成目的(如图1所示),而重链的正确联结可利用KiH、静电转向技术达成。
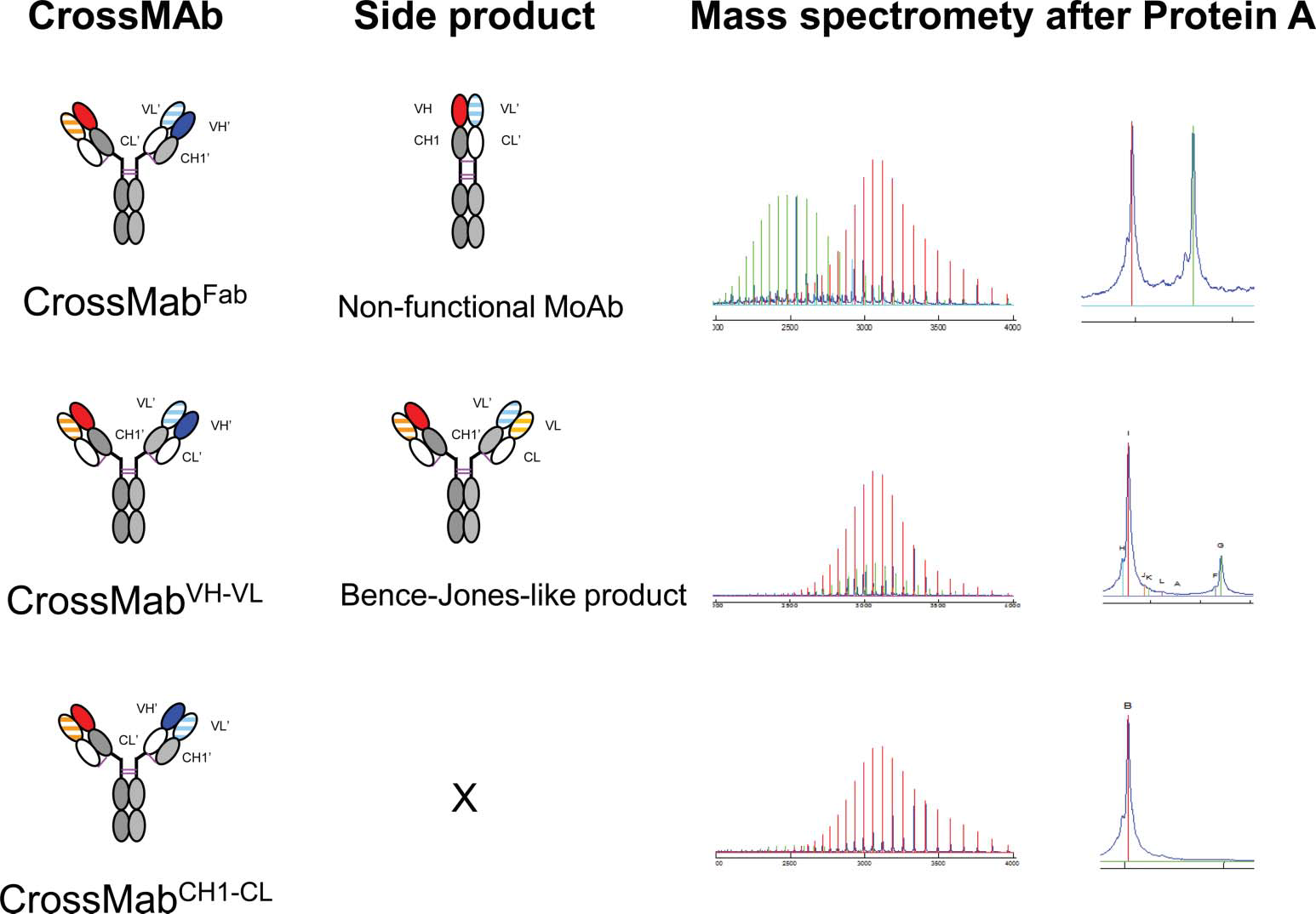
图1:3种主要的CrossMAb形式:CrossMAbFab、CrossMAbVH-VL 、CrossMAbCH1-CL及其推测的副产物
实践证明CrossMAb已经成了具有广泛用途的抗体工程技术之一,可用于多种形式双特异抗体的构建(如图2所示),如二价(1+1)、三价(2+1)、四价(2+2)双特异抗体等,还可以将2个抗原结合片段Fab串联在一起,抗体的配对通过功能域的交换达成,而不需要相应轻链的确证、翻译后处理或体外化学组装、引入适于正确联结的突变等。许多学术研究者成功验证了该方法的可靠性,其中有4种独特设计的双特异抗体已经进入了I/II期临床试验(见图3)。可采用成熟的上下游工艺流程用CHO细胞制备,其规模、产量、糖基化、稳定性和质量可媲美传统IgG抗体。
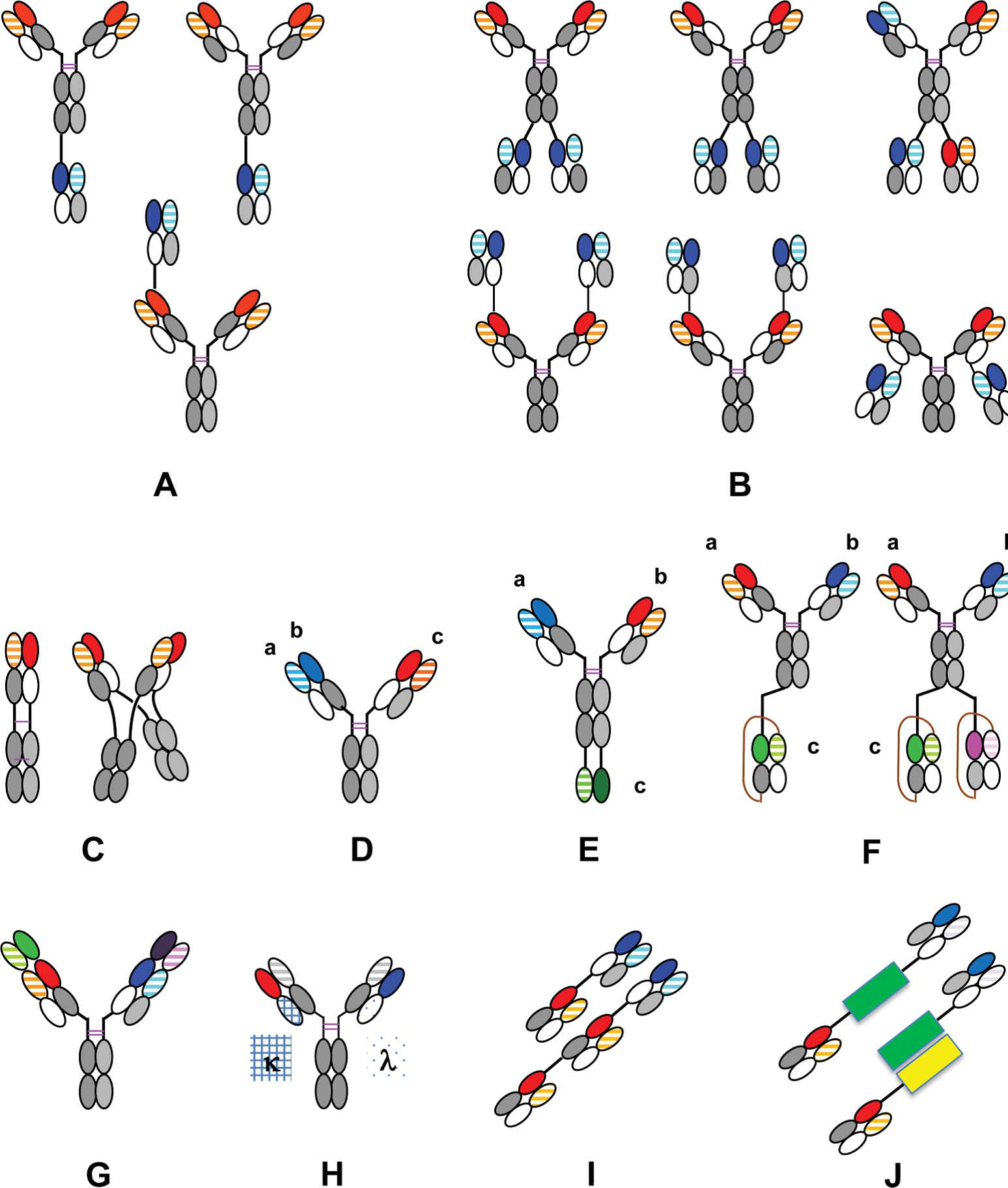
图2:CrossMAb的各种形式
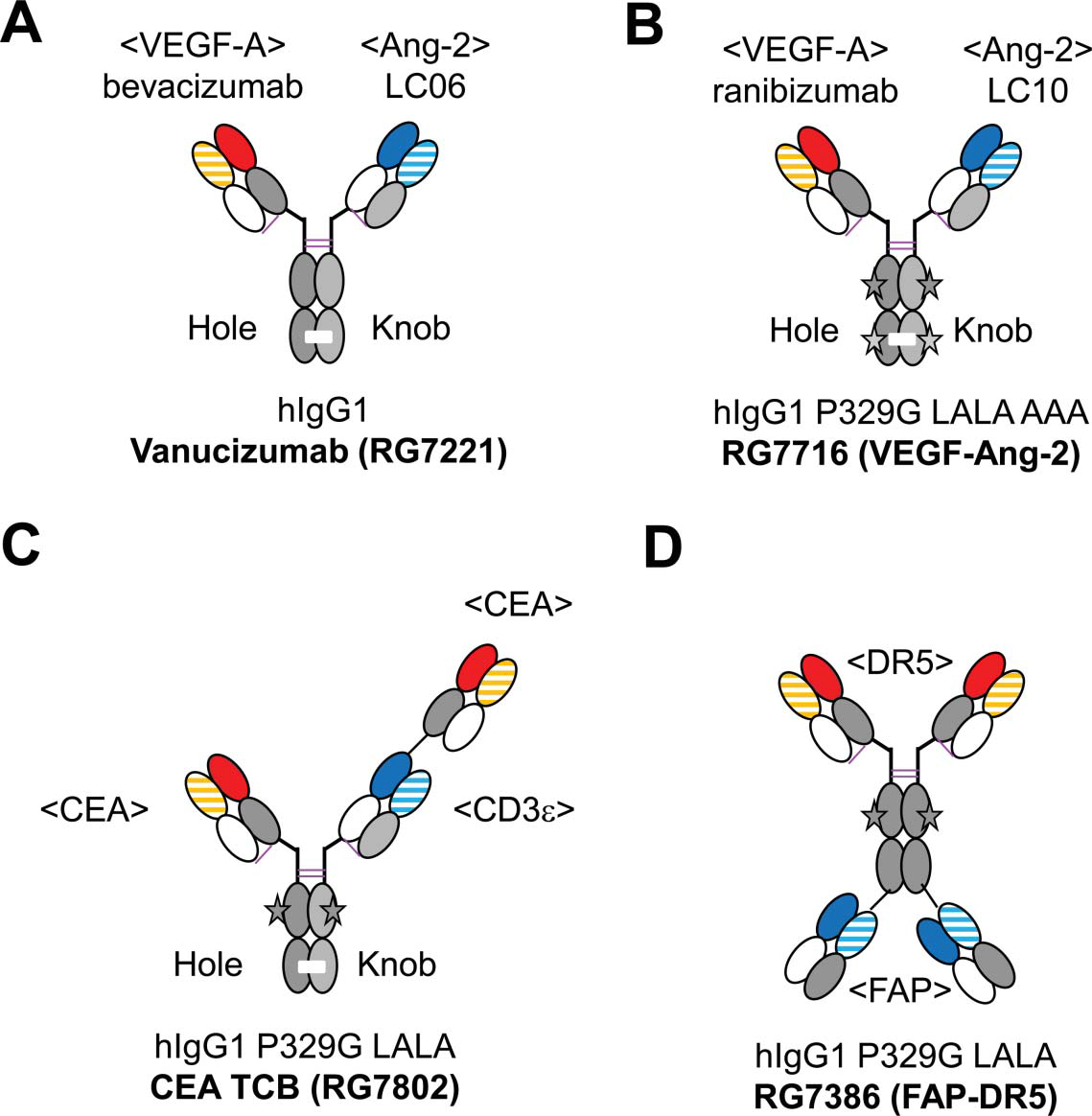
图3:进入临床试验的CrossMAb抗体
携带CH1-CL链交换的双特异CrossMAb抗体设计原理如图4所示,鉴于VH、 Vk 和Vλ功能域以及对应的恒定区结构相似,设计出了交叉点序列。通过对曲妥珠单抗(PDB:1N8Z)的VH、VL(kappa)、CH1、CL(Kappa)以及Lamda Fab(PDB: 7FAB )的VL(Lamda)、CL(Lamda)等晶体结构的分析总结,发现3个可变区功能域和3个恒定区功能域独立行使功能,依赖于邻近肘部的空间结构上匹配的β-片层叠加区域。

图4:携带CH1-CL的CrossMAbs的设计方案
在CrossMAb技术的基础上,进一步发展出一些不同于CrossMAb的抗体工程技术用以产生双特异抗体,如DVD-IgG和 CODV-Ig技术等,形成双体、双功能Fabs (DAFs)、Dutafabs等形式,极大地丰富了双特异抗体构建策略,为其应用奠定了基础。
一孔之见:CrossMAb技术作为设计双特异抗体的一种策略,虽然解决了轻链正确联结的问题,但可能的副产品难以避免,还需要与KiH等相关技术联合应用才能取得较好效果,产业化问题是限制其实际应用的关键。
本文内容来源:拜西欧斯(北京)生物技术有限公司
更多精彩内容请登陆(拜西欧斯)官方网站:www.biocells.cn

 )
)






























我来说两句排行榜